CAR-T療法(キメラ抗原受容体T細胞療法)は、再発・難治性の血液がんに対する画期的な治療法として、臨床現場での導入が急速に進んでいますね。しかし、その強力な抗腫瘍効果の一方で、サイトカイン放出症候群(CRS)や神経毒性(ICANS)といった、特有かつ致死的な副作用管理が大きな課題となっています。これらの副作用は進行が早く、適切なタイミングでの介入が遅れると患者さんの予後に直結するため、医療チーム全体での共通認識と迅速な対応が不可欠です。
本記事では、最新のASTCTコンセンサスグレードに基づいた重症度評価や、トシリズマブ・ステロイドを用いた実践的な治療アルゴリズムについて、現場の医療従事者向けに詳しく解説します。安全なCAR-T療法実施のための体制構築にお役立てください。
CAR-T療法の副作用管理における結論:ASTCT分類に基づく早期発見と迅速な介入

CAR-T療法の副作用管理において最も重要な結論は、ASTCT(米国移植細胞治療学会)分類などの国際的な基準に基づき、早期発見と迅速な介入を行うことです。CRSやICANSは、発現から重症化までのスピードが非常に速い場合があります。そのため、個人の経験則に頼るのではなく、標準化されたプロトコルに沿ってチーム全体で動くことが、患者さんの安全を守る鍵となります。ここでは、管理の全体像とガイドライン準拠の重要性について確認していきましょう。
CRS・ICANS管理の全体像と治療ゴール
CRSおよびICANS管理の最大のゴールは、副作用を可逆的な段階でコントロールし、永続的な臓器障害や致死的な転帰を防ぐことです。CAR-T細胞が体内で増殖し、がん細胞を攻撃する過程で生じる免疫反応は治療効果の裏返しでもありますが、過剰な炎症は抑制しなければなりません。
具体的には、バイタルサインや神経所見の微細な変化を見逃さず、グレードに応じた治療介入を遅滞なく行うことが求められます。特にICANSは不可逆的な脳損傷につながるリスクがあるため、早期の神経学的評価が極めて重要です。治療効果を最大限に維持しつつ、毒性を最小限に抑えるバランス感覚が、私たち医療従事者には求められているのです。
重症化を防ぐためのガイドライン準拠とアルゴリズムの重要性
副作用の重症化を防ぐためには、ASTCTコンセンサスグレードなどのガイドラインに準拠した管理が不可欠です。施設ごとに独自の基準で判断してしまうと、対応の遅れや過剰投与につながる恐れがあるからです。明確なアルゴリズムを導入することで、医師、看護師、薬剤師が共通言語で患者状態を把握できるようになります。
例えば、「発熱が続いているが様子を見よう」といった曖昧な判断を排除し、「グレード1のCRSとして対症療法を開始し、グレード2への移行を監視する」といった具体的なアクションプランへ落とし込むことが大切です。アルゴリズムに沿ったシステマチックな対応こそが、安全管理の基盤となるでしょう。
CRS・ICANSの発現メカニズムとリスク因子

適切な管理を行うためには、なぜこれらの副作用が起こるのか、そのメカニズムを理解しておくことが大切です。CAR-T細胞が標的抗原を認識した際に引き起こされる免疫反応の連鎖が、全身性の炎症や神経症状へとつながります。ここでは、病態生理とリスク因子、そして製剤ごとの特徴について解説します。
CAR-T細胞の活性化と炎症性サイトカイン放出の病態
CRS(サイトカイン放出症候群)は、体内に輸注されたCAR-T細胞が腫瘍抗原を認識して活性化・増殖する過程で、大量の炎症性サイトカインが放出されることで発症します。特にインターロイキン-6(IL-6)、インターフェロン-γ(IFN-γ)、TNF-αなどが主要なメディエーターとして知られています。
この「サイトカイン・ストーム」とも呼ばれる過剰な免疫反応は、高熱、低血圧、低酸素血症などの全身症状を引き起こします。マクロファージや内皮細胞も活性化され、炎症の連鎖が増幅されるのです。腫瘍量が多い場合や、CAR-T細胞の急激な増殖が見られる症例では、より重篤なCRSが発現しやすい傾向にあります。
血液脳関門(BBB)の破綻と神経毒性発現の機序
ICANS(免疫エフェクター細胞関連神経毒性症候群)の発症には、血液脳関門(BBB)の破綻が深く関与していると考えられています。全身性の炎症によりBBBの透過性が亢進し、サイトカインや活性化したリンパ球が中枢神経系へ流入することで神経障害が引き起こされます。
これにより、脳浮腫や脳症のような症状が現れます。特にIL-6やIL-1などのサイトカインレベルの上昇は、神経毒性の重症度と相関することが報告されています。BBBを構成する周皮細胞の障害も指摘されており、血管内皮の活性化と凝固異常が複雑に絡み合って神経症状を発現させるのです。
製剤による副作用発現率の違いと好発時期のタイムライン
使用するCAR-T製剤の構造、特に共刺激ドメインの違い(4-1BBかCD28か)によって、副作用の発現率や時期(タイムライン)が異なります。一般的に、CD28ドメインを持つ製剤(イエスカルタなど)は増殖が急速で、投与後早期(数日以内)にCRSやICANSが発現しやすい傾向があります。
一方、4-1BBドメインを持つ製剤(キムリア、ブレヤンジなど)は、比較的緩やかに増殖するため、発現時期がやや遅く、ピークが投与後1週間前後になることもあります。各製剤の特性を把握し、いつ頃リスクが高まるかを予測してモニタリング体制を強化することが、臨床現場での重要なポイントです。
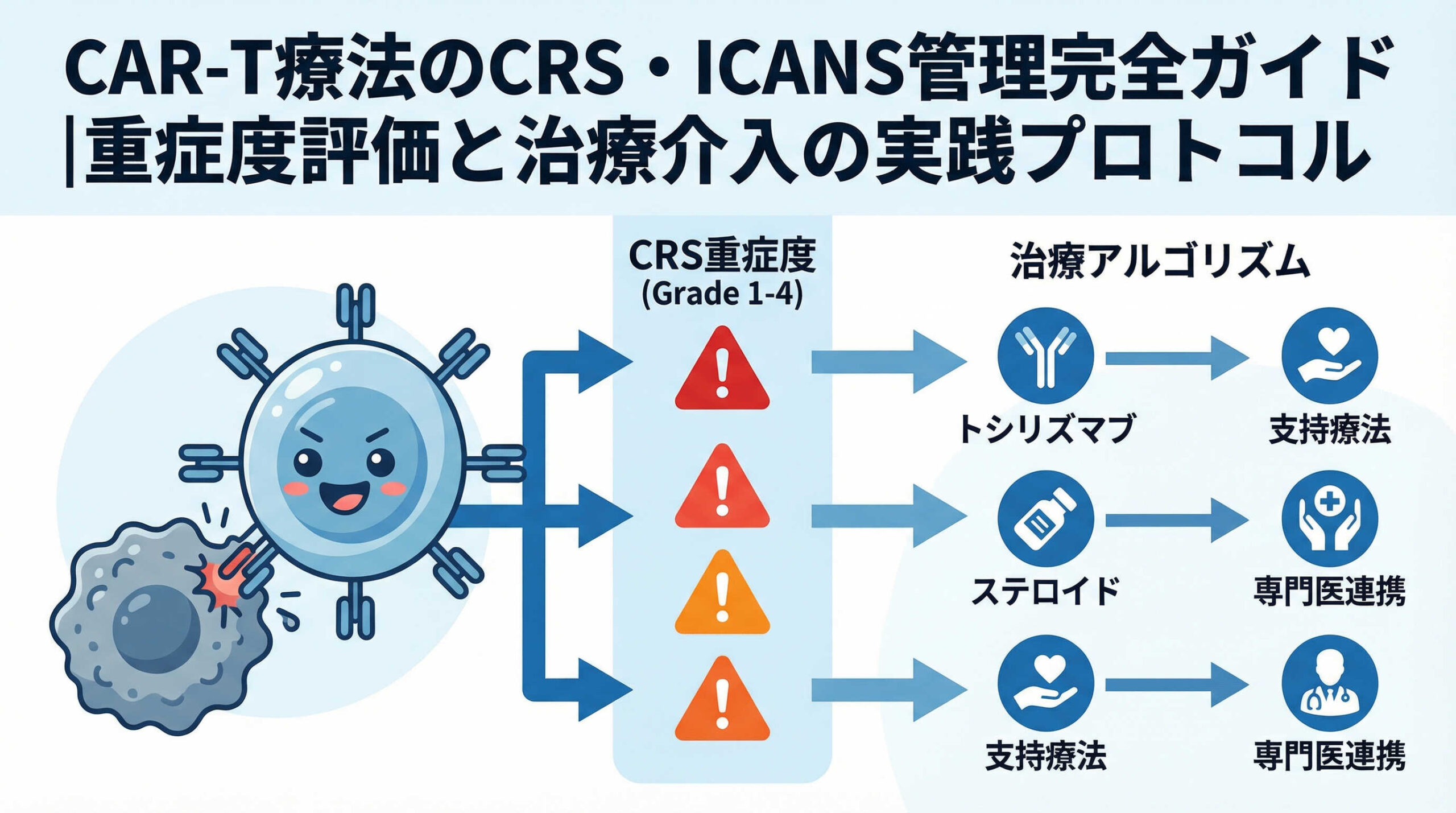
CRS(サイトカイン放出症候群)の重症度評価(グレーディング)と具体的対応

CRS管理の実践において中心となるのが、ASTCTコンセンサスグレードに基づいた重症度評価と、それに応じた段階的な治療介入です。発熱のみの軽症例から、生命維持処置を要する重症例まで、グレードごとに対応は明確に定められています。ここでは、各グレードの定義と具体的な対応策、そしてトシリズマブやステロイドの使用法について詳しく見ていきましょう。
ASTCTコンセンサスグレードに基づくCRS評価基準
ASTCTのコンセンサスグレード分類は、発熱、低血圧、低酸素血症の3要素に基づいてCRSの重症度を決定する世界的な標準基準です。この分類を正確に適用することで、過不足のない治療介入が可能となります。以下に各グレードごとの具体的な定義と、臨床現場で求められる対応方針を整理しました。
Grade 1:発熱(38.0℃以上)のみの管理方針
Grade 1は、38.0℃以上の発熱があるものの、低血圧や低酸素血症を伴わない状態です。この段階では、基本的に対症療法が中心となります。アセトアミノフェンなどの解熱剤を使用し、水分補給を行いながら注意深く観察します。ただし、高齢者や併存疾患がある場合は、早期のトシリズマブ投与を検討することもあります。感染症との鑑別のための培養検査もこの時点で行いましょう。
Grade 2:低血圧・低酸素血症への輸液・酸素投与
Grade 2は、発熱に加え、輸液のみで反応する低血圧、または低流量酸素(カニューラ等で6L/分以下)を要する低酸素血症がある状態です。ここでは積極的な介入が必要です。輸液負荷を行っても血圧が安定しない場合や酸素需要が増加する場合は、トシリズマブの投与を開始します。患者さんの全身状態が悪化する前に、炎症の連鎖を断ち切ることが重要です。
Grade 3:昇圧剤・高流量酸素が必要な場合の対応
Grade 3は、昇圧剤(単剤または複数)の使用が必要な低血圧、あるいは高流量酸素や非侵襲的陽圧換気(NPPV)を要する低酸素血症を指します。この段階は重症であり、ICUでの管理が望ましいでしょう。トシリズマブの投与に加え、デキサメタゾンなどのコルチコステロイドの併用を強く推奨します。迅速に炎症を鎮静化させなければ、多臓器不全へ進行するリスクが高まります。
Grade 4:生命維持処置を要する緊急対応
Grade 4は、複数の昇圧剤を使用しても血圧維持が困難な場合や、人工呼吸器管理(挿管)を要する低酸素血症がある、生命を脅かす状態です。直ちに最大強度の治療介入が必要です。トシリズマブと高用量ステロイドの併用はもちろん、場合によってはシクロホスファミドなどの追加免疫抑制療法も検討されます。集学的治療体制で救命にあたることが最優先されます。
トシリズマブ(抗IL-6受容体抗体)の投与プロトコルと反復投与
トシリズマブ(抗IL-6受容体抗体)は、CRS治療のキードラッグです。通常、成人では体重あたり8mg/kg(最大800mg)を1回投与量とします。重要なのは、効果不十分な場合の反復投与の判断です。初回投与後、8時間経過しても症状の改善が見られない場合は、追加投与が可能です。
添付文書上は最大3〜4回までの投与が認められていますが、漫然と繰り返すのではなく、ステロイドの併用や増量を並行して検討する必要があります。トシリズマブはCRSの症状を劇的に改善させる可能性がありますが、投与のタイミングを逸しないよう、薬剤部との連携による迅速な払い出し体制を整えておくことが大切ですね。
コルチコステロイドの併用タイミングと減量計画
コルチコステロイド(デキサメタゾンやメチルプレドニゾロン)は、トシリズマブ不応例や重症CRS(Grade 3以上)、またはICANS併発時に使用されます。かつてはCAR-T細胞の効果を減弱させる懸念から使用が控えられていましたが、現在は早期かつ短期間の使用であれば抗腫瘍効果への影響は限定的であるという見方が一般的です。
投与開始後は、症状の改善を見ながら数日かけて慎重に減量(テーパリング)していきます。急激な中止はCRSの再燃を招くリスクがあるためです。減量計画は患者さんの反応を見ながら柔軟に調整し、副作用と治療効果のバランスを見極めることが肝要です。
敗血症など感染症との鑑別診断におけるポイント
CRSの症状である発熱や低血圧は、敗血症などの重症感染症と非常に類似しています。CAR-T療法を受ける患者さんは高度な免疫不全状態にあるため、感染症のリスクも常に抱えています。そのため、発熱時にはCRSと決めつけず、必ず血液培養などの感染症ワークアップを行うことが鉄則です。
臨床的には、広域スペクトルの抗菌薬を予防的あるいは経験的に投与しながら、CRS治療を進める「double cover」の戦略がとられることが一般的です。CRPやフェリチンなどの炎症マーカーの推移に加え、プロカルシトニンなども参考にしながら、感染症の可能性を除外しない慎重な姿勢が求められます。
ICANS(神経毒性)のスクリーニング手法と治療戦略

ICANS(神経毒性)は、CRSとは異なるアプローチが必要です。初期症状が軽微であっても急速に意識障害や痙攣へと進行することがあるため、特有のスクリーニング手法を用いた定点観測が欠かせません。ここでは、ICEスコアを用いた評価法や、デキサメタゾンを中心とした治療戦略、そしてICANS特有の注意点について解説します。
ICEスコア(Immune Effector Cell-Associated Encephalopathy Score)を用いた評価法
ICANSの早期発見には、ICEスコア(Immune Effector Cell-Associated Encephalopathy Score)を用いた評価が標準的です。これは10点満点のスコアリングシステムで、見当識(年・月・場所・病院名)、命名(物品の名前)、命令(指示動作)、書字(文章を書く)、注意(数字の逆唱)の5項目を評価します。
特に「書字」の変化は、他の症状より先に現れることが多く、感度の高い指標として知られています。毎日同じ文章を書いてもらい、筆跡の乱れや字の崩れがないかを確認することが、早期発見のコツです。看護師による日々の観察が、ICANSの兆候を捉える上で非常に大きな役割を果たします。
ASTCTコンセンサスグレードに基づくICANS重症度分類
ICANSの重症度もASTCTコンセンサスグレードに基づいて分類されます。基本的にはICEスコアの点数と意識レベルによって決定されます。ICEスコアが7〜9点はGrade 1、3〜6点はGrade 2、0〜2点はGrade 3と定義され、Grade 4は昏睡状態や重篤な痙攣発作などを指します。
このグレード分類は、治療介入のトリガーとなります。例えば、Grade 2以上になった時点でステロイド投与を開始するなど、客観的な数値に基づいて判断することで、治療の遅れを防ぐことができます。意識レベルの低下(覚醒度)も重要な要素ですので、JCSやGCSと合わせて評価しましょう。
デキサメタゾンを中心としたICANS治療アルゴリズム
ICANS治療の第一選択薬は、血液脳関門を通過しやすいデキサメタゾンなどのステロイドです。ICANSは脳浮腫を伴うことがあるため、強力な抗炎症作用を持つステロイドが有効です。一般的にGrade 2以上のICANSに対して投与が推奨されています。
投与量は重症度に応じて調整しますが、例えばデキサメタゾン10mgを6時間ごとに投与し、症状改善後に漸減していくプロトコルが多く用いられます。ステロイドの使用はCAR-T細胞への影響が懸念されますが、神経毒性は不可逆的な後遺症を残す可能性があるため、躊躇せず十分量を使用することが推奨されています。
抗てんかん薬(レベチラセタム等)の予防投与と発作時対応
ICANSに伴う痙攣発作は、誤嚥や低酸素脳症を引き起こす危険な合併症です。そのため、CAR-T細胞輸注開始時から、レベチラセタムなどの抗てんかん薬を予防的に投与することが多くの施設で行われています。予防投与により、発作のリスクを低減できると考えられています。
もし実際に発作が起きてしまった場合は、ベンゾジアゼピン系薬剤などで直ちに発作を停止させ、気道確保を行うとともに、ICANSのグレードをGrade 3または4として扱い、高用量ステロイドによる治療を強化します。神経内科医と連携し、脳波検査などで発作波の有無を確認することも重要です。
ICANS単独発現時におけるトシリズマブ使用の禁忌と注意点
非常に重要な注意点として、CRSを伴わないICANS単独の発現に対しては、トシリズマブの投与は推奨されません。むしろ症状を悪化させるリスクがあるため、原則として禁忌に近い扱いとなります。これは、トシリズマブが末梢血中のIL-6受容体を塞ぐことで、血清IL-6濃度が一過性に上昇し、それが血液脳関門を通過して中枢神経系内の炎症を増悪させる可能性があるためです。
ICANS単独の場合はステロイドが治療の主役です。ただし、CRSとICANSが合併している場合は、CRS治療のためにトシリズマブを使用することは許容されます。この使い分けは専門的な判断が必要ですので、アルゴリズムをよく確認しましょう。
臨床現場における副作用モニタリング体制と多職種連携

CAR-T療法は、医師だけでなく、看護師、薬剤師、コメディカルを含めた多職種チームでの総力戦です。副作用の兆候をいち早くキャッチし、シームレスに治療へつなげるためには、職種を超えた連携体制の構築が欠かせません。ここでは、各職種の役割と連携のポイントについて具体的に解説します。
看護師によるバイタルサイン測定と書字確認等の神経学的観察
看護師は、患者さんのベッドサイドで最も多くの時間を過ごすため、副作用の第一発見者となることが多い重要なポジションです。通常のバイタルサイン測定に加え、ICEスコアの評価を定時で行い、微細な神経症状の変化を見逃さないことが求められます。
特に「書字確認」は、会話だけでは気づきにくい高次脳機能障害を捉えるのに有効です。また、患者さんの言動が「いつもと違う」「つじつまが合わない」といった違和感は、ICANSの初期徴候である可能性が高いため、些細なことでも医師へ報告する文化を作ることが大切です。患者さんの不安に寄り添う精神的なケアも、看護師の大きな役割ですね。
薬剤師によるトシリズマブの在庫管理と緊急払い出し体制
CRS治療薬であるトシリズマブは、投与が必要と判断されたら「直ちに」使用できる状態でなければなりません。数時間の遅れが重症化につながることもあるため、薬剤師による在庫管理は生命線とも言えます。夜間や休日を含め、オーダーから投与開始までの時間を最小限にするための緊急払い出しフローを確立しておく必要があります。
また、併用薬の相互作用チェックや、ステロイドの減量スケジュールの管理においても、薬剤師の専門性は不可欠です。副作用治療薬が確実に届くロジスティクスを整えることは、CAR-T療法の安全性を担保する基盤となります。
集中治療室(ICU)および神経内科専門医との連携フロー
重症CRSやICANSが発現した場合、血液内科医だけでの対応は困難になります。循環動態が不安定な場合は集中治療室(ICU)での全身管理が、難治性の痙攣や意識障害がある場合は神経内科専門医による評価が必要となります。
トラブルが起きてから依頼するのではなく、治療開始前からICUや他科の医師と情報を共有し、「どのような状態になったら転科・併診するか」という連携フローを事前に合意しておくことがスムーズな診療につながります。院内全体でCAR-T療法を支えるバックアップ体制を整えておくことが安心材料になります。
患者・家族への退院指導と緊急時の連絡体制
CAR-T療法の副作用は、退院後に遅発性に現れることは稀ですが、血球減少や感染症リスクは続きます。また、万が一の神経症状の再燃などに備え、患者さんとご家族への退院指導は丁寧に行う必要があります。
「熱が出たらすぐに連絡する」「ろれつが回らない等の症状があれば救急受診する」といった具体的なアクションを指導し、緊急時の連絡先カード(ウォレットカード)を常に携帯してもらうようにしましょう。自宅での生活に戻った後も、医療機関とすぐにつながれる安心感を提供することが、長期的なフォローアップにおいて重要です。
まとめ

CAR-T療法の副作用管理(CRS・ICANS)について解説してきました。最も重要なのは、ASTCTグレード分類などの客観的な基準に基づき、チーム全体で早期発見・早期介入を行うことです。CRSにはトシリズマブ、ICANSにはステロイドという治療の基本を押さえつつ、ICEスコアによるモニタリングや多職種連携を徹底することで、重篤な事態を回避できます。最新の知見と院内プロトコルを常に照らし合わせ、安全で効果的な治療を提供していきましょう。
CAR-T療法の副作用管理(CRS・ICANS)についてよくある質問

以下のFAQリストは、CAR-T療法の副作用管理に関するよくある質問と回答をまとめたものです。
- CRSとICANSの発現時期にはどのような違いがありますか?
- 一般的に、CRSはCAR-T細胞輸注後1〜5日程度の早期に発現することが多く、ICANSはCRSの発現後、あるいはCRSの回復期(輸注後4〜10日頃)に発現する傾向があります。ただし、製剤の種類や患者背景により異なります。
- トシリズマブを投与してもCRSが改善しない場合、次の一手は?
- トシリズマブ投与後も改善が見られない場合、あるいは重症化する場合は、デキサメタゾンやメチルプレドニゾロンなどのコルチコステロイドの併用を開始します。それでも制御困難な場合は、高用量ステロイドパルス療法や他の免疫抑制剤を検討します。
- なぜICANS単独の発症に対してトシリズマブを使用してはいけないのですか?
- トシリズマブが末梢血中のIL-6受容体をブロックすることで、血中のIL-6濃度が一過性に上昇し、それが血液脳関門(BBB)を通過して中枢神経系内の炎症を悪化させるリスクがあるためです。
- 退院後も副作用のリスクは続きますか?
- CRSやICANSの急性期リスクは退院時には消失していることがほとんどですが、B細胞無形成に伴う低ガンマグロブリン血症や、遷延する血球減少による感染症リスクは長期にわたって続くため、継続的なフォローアップが必要です。
- 施設で副作用対応マニュアルを作成する際のポイントは?
- ASTCTグレード分類をそのまま引用するだけでなく、自施設の設備(ICUへの動線、薬剤部の夜間体制など)に合わせた具体的なアクションフロー(「誰に連絡するか」「どこで治療するか」)を明記することが、実効性のあるマニュアル作成のコツです。