CAR-T細胞療法の製造プロセスは、高度なバイオテクノロジーと厳格な品質管理が求められる複雑な工程の連続です。新規プロジェクトの立ち上げや既存プロセスの見直しを担当される皆様にとって、各工程におけるリスク管理やコスト削減、品質の安定化は喫緊の課題ではないでしょうか。
本記事では、CAR-T製造プロセスの全容を、技術的な視点から詳細に解説いたします。「Vein-to-Vein」の流れから、分離・遺伝子導入・培養といった各単位操作の技術的ポイント、さらには品質管理(QC)の重要項目までを網羅しました。また、自動化や閉鎖系への移行といった最新のプロセス最適化トレンドについても触れています。実務に直結する専門知識を整理し、より効率的で堅牢な製造体制の構築にお役立てください。
CAR-T製造プロセスの全体像と標準的ワークフロー

CAR-T細胞療法は、患者自身の細胞を加工して治療に用いる「オーダーメイド医療」の極致と言えます。そのため、製造プロセスは単なる細胞培養ではなく、厳密に管理されたロジスティクスと製造工程が一体となったワークフローとして理解する必要があります。ここでは、全体的な流れと基本的な概念について整理しましょう。
患者からの採血から投与までのVein-to-Veinプロセス
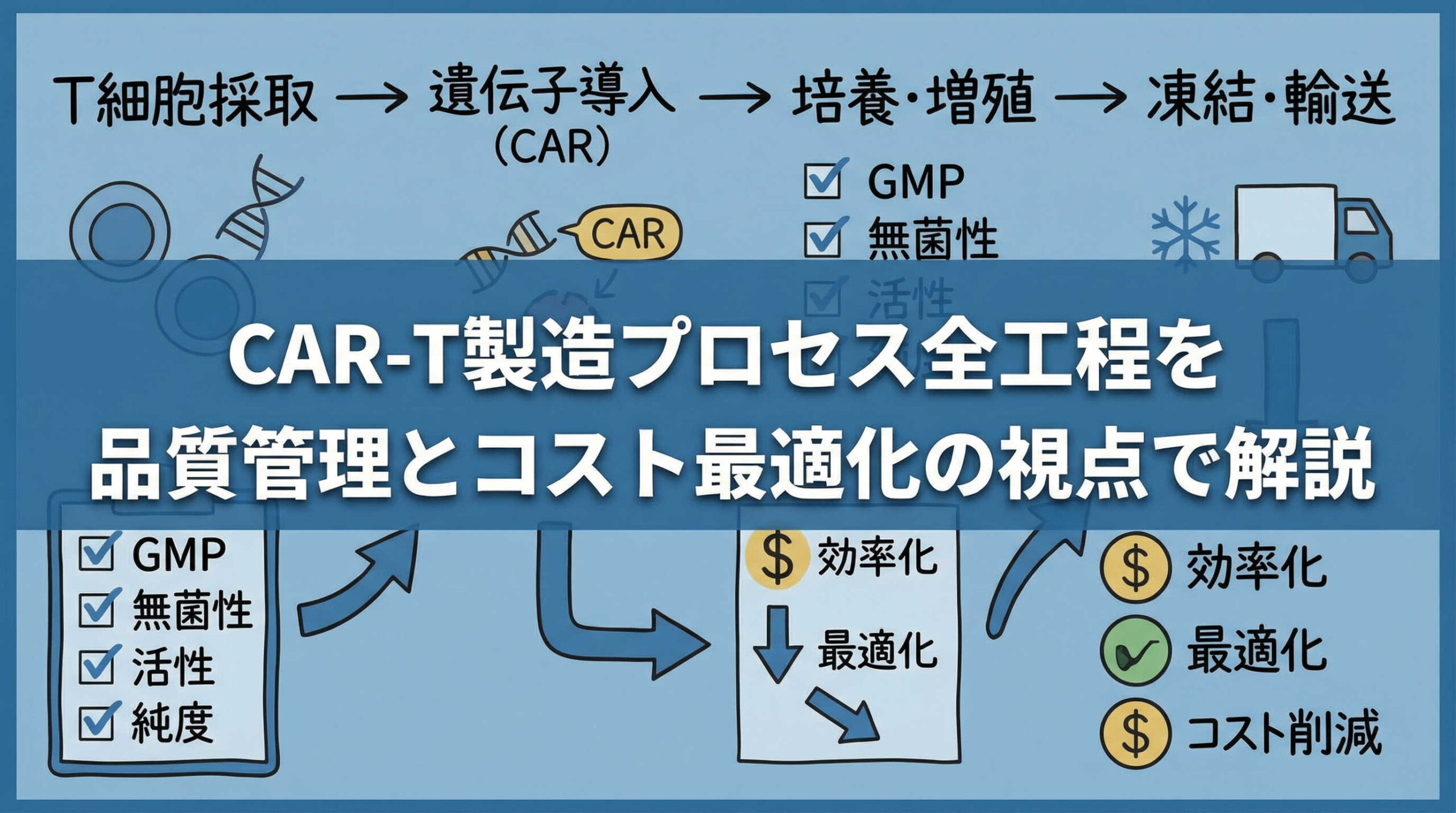
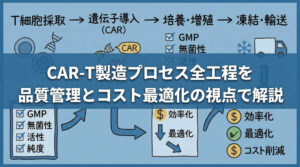
CAR-T療法における製造プロセスは、患者から細胞を採取し、最終的に患者へ投与するまでの一連の流れを指す「Vein-to-Vein(静脈から静脈へ)」という概念で捉えられます。このプロセスは、医療機関と製造施設の間で厳密な連携が必要となります。
- アフェレーシス(成分採血): 医療機関にて患者から白血球成分を採取
- 輸送: 温度管理された状態で製造施設へ輸送(低温または凍結)
- 製造(加工): 選別、活性化、遺伝子導入、拡大培養など
- 製剤化・凍結: 最終製品として調製し凍結保存
- 輸送・保管: 医療機関へ返送し、投与まで保管
- 投与: 患者への輸注
この全工程において、個体識別管理(Chain of Identity)と保管温度管理(Chain of Custody)の維持が不可欠です。
自家CAR-T療法における製造タイムラインの目安
自家CAR-T療法の場合、アフェレーシスから最終製品の出荷判定(リリース)まで、一般的に2週間から3週間程度の期間を要します。製造工程自体は技術の進歩により短縮化の傾向にありますが、品質試験に一定の時間を要するためです。
- 準備・輸送(1-2日): 採取および施設への搬入
- 製造工程(7-10日): 活性化、遺伝子導入、拡大培養
- 製剤化・試験(3-7日): 充填、無菌試験等の品質確認
- 出荷判定・輸送(1-2日): QAレビュー完了後の出荷
近年では、培養期間を短縮する「Fast CAR-T」等の技術開発も進んでおり、将来的にはさらに短いタイムラインでの提供が可能になるでしょう。
製造工程におけるGMP要件と「Process is the Product」の概念
再生医療等製品、特に細胞加工製品においては、「Process is the Product(プロセスこそが製品である)」という重要な概念があります。低分子医薬品とは異なり、最終製品の品質を完全に均一化することが難しいため、製造プロセスの堅牢性がそのまま製品の品質と安全性に直結するという考え方です。
したがって、GMP(Good Manufacturing Practice)省令に基づいた厳格な製造管理および品質管理が求められます。原材料の受け入れから製造環境の清浄度管理、作業者のトレーニングに至るまで、プロセス全体がバリデートされた状態で運用されなければなりません。わずかな手順の変更が、細胞の表現型や活性に予期せぬ影響を与える可能性があるため、変更管理(Change Control)も極めて慎重に行う必要があります。
CAR-T製造の各工程における作業内容と技術的ポイント

製造プロセスの中心となるのは、採取したT細胞にCAR(キメラ抗原受容体)遺伝子を導入し、治療に必要な数まで増幅させる一連の細胞加工操作です。各ステップには特有の技術的課題と、品質を左右する重要なポイントが存在します。ここでは工程順に詳細を解説します。
原材料の受け入れ:アフェレーシス産物の品質確認
製造施設に到着したアフェレーシス産物は、直ちに受け入れ検査が行われます。ここでの品質が、その後の製造成功率を大きく左右するためです。外観確認、バッグの破損有無、ラベルの照合に加え、細胞数や生存率の測定が行われます。
特に、患者は化学療法を受けていることが多く、T細胞の数や質が低下しているケースが少なくありません。開始時点でのCD3陽性細胞数やCD4/CD8比率、単球(Monocytes)の混入率などを把握し、必要に応じてプロセスの微調整を行う判断が求められることもあります。トレーサビリティ確保のため、受入時のデータ記録は極めて重要です。
T細胞の分離・選別:密度勾配遠心法と磁気ビーズ法の活用
アフェレーシス産物にはT細胞以外にも赤血球、血小板、単球などが含まれているため、目的とするT細胞を純化する必要があります。
- 密度勾配遠心法: Ficollなどを用いて単核球層を分離する古典的な手法ですが、自動化装置(Sepax等)を用いることで閉鎖系での処理が可能です。
- 磁気ビーズ法: 抗CD3や抗CD4/CD8抗体が結合した磁気ビーズ(CliniMACS等)を用いて、特定の細胞集団をポジティブ選別またはネガティブ選別します。
近年では、より純度の高いT細胞を得るために、磁気ビーズによる選別が標準的になりつつあります。これにより、後の工程での導入効率や増殖効率の向上が期待できます。
T細胞の活性化:抗CD3/CD28抗体ビーズ等による刺激
分離したT細胞は、静止期(G0期)にあることが多いため、遺伝子導入や増殖を促すために活性化させる必要があります。生理的なT細胞活性化シグナルを模倣するため、抗CD3抗体および抗CD28抗体を用いるのが一般的です。
具体的には、これらの抗体を結合させた磁気ビーズ(Dynabeads等)を添加し、細胞と共培養します。この刺激によりT細胞は細胞周期に入り、分裂増殖を開始するとともに、ウイルスベクターによる遺伝子導入を受け入れやすい状態になります。活性化の強さや期間は、最終的な細胞のメモリーフェノタイプ(Tcm, Temなど)に影響を与えるため、厳密な制御が必要です。
遺伝子導入:ウイルスベクターを用いたCAR遺伝子の導入効率
CAR-T製造の核心部分である遺伝子導入には、主にレンチウイルスベクターやレトロウイルスベクターが用いられます。活性化したT細胞にウイルス液を添加し、CAR遺伝子をゲノムに組み込ませます。
- MOI(Multiplicity of Infection): 細胞1個あたりのウイルス粒子の比率。コストと導入効率のバランスを見て最適化します。
- 導入効率(Transduction Efficiency): 通常、数10%〜数10%程度の陽性率を目指します。
- スピンオキュレーション: 遠心力を利用してウイルスと細胞の接触頻度を高め、導入効率を向上させる手法も採用されます。
ウイルスの品質(力価)や添加タイミングは、製造の再現性に大きく関わる重要管理点です。
拡大培養:バイオリアクターを用いた細胞増殖と代謝制御
遺伝子導入後、治療に必要な細胞数(数億〜数十億個)を確保するために拡大培養を行います。ここでは、ガス交換効率や栄養供給に優れた培養装置の選択が重要です。
- Wave Bioreactor: 揺動式のバッグ培養装置。十分な酸素供給が可能で、大規模培養に適しています。
- G-Rex: ガス透過性の底面を持つ静置培養容器。培地交換の手間を減らし効率的に培養できます。
培養中は、グルコース消費や乳酸産生、pH、溶存酸素などをモニタリングし、細胞の代謝状態を制御します。過度な増殖による細胞の疲弊(Exhaustion)を防ぐため、適切なタイミングで培養を終了することが肝要です。
細胞洗浄・濃縮:不純物除去と培地成分の置換
目標とする細胞数に達したら、最終製品としての純度を高めるために洗浄と濃縮を行います。培養液に含まれる血清成分、サイトカイン、代謝老廃物、そして活性化に使用した磁気ビーズを除去する必要があります。
特に磁気ビーズの除去は安全性に関わるため、専用の磁石装置を用いて確実に行います。その後、自動遠心装置などを用いて細胞を洗浄し、最終的な製剤化用の保存液へと置換します。この工程での細胞回収率の低下を防ぐため、処理速度や遠心条件の最適化が重要です。
最終製剤化:凍結保存液への懸濁と充填作業
洗浄・濃縮された細胞は、最終的な投与用バッグやバイアルに充填されます。この工程は製品の無菌性を担保するため、特に厳格な環境下(グレードA等)で行われるか、完全閉鎖系で行われます。
細胞懸濁液にDMSO(ジメチルスルホキシド)などの凍結保護剤を含む保存液を添加し、規定の細胞密度に調整します。充填後は、ラベルの貼付や外観検査を行い、速やかに凍結工程へと移行します。DMSOは室温で細胞毒性を示すため、添加から凍結開始までの時間管理(Hold Time)は極めてシビアに設定する必要があります。
凍結保存:プログラムフリーザーを用いた温度管理と保管
充填された製品は、細胞の生存率を維持するために制御された速度で冷却(通常-1℃/min)する必要があります。これにはプログラムフリーザーを使用します。
冷却後、気相液体窒素タンク(-150℃以下)にて保管します。保管中の温度逸脱は製品の品質劣化に直結するため、24時間体制のモニタリングシステムによる監視が必須です。出荷時もドライシッパー等の専用容器を用い、極低温状態を維持したまま医療機関へ輸送されます。
製造プロセスにおける品質管理(QC)と重要管理点

CAR-T製品は生きた細胞であるため、その品質は原料の状態や製造工程の変動に影響を受けやすくなります。そのため、厳格な品質管理(QC)戦略が不可欠です。安全性、純度、効力(ポテンシー)を保証するために実施される主要な試験項目について解説します。
工程内管理(IPC)におけるモニタリング項目
最終製品の試験だけでなく、製造途中の段階でプロセスが順調に進んでいるかを確認するのが工程内管理(IPC: In-Process Control)です。
- 細胞数・生存率: 各工程の前後で測定し、増殖曲線や回収率を確認します。
- pH・ガス分圧: 培養環境が適切かモニタリングします。
- グルコース・乳酸: 代謝活性の指標として測定します。
これらのデータを蓄積し、トレンド分析を行うことで、プロセスの異常を早期に検知し、製品ロスのリスクを低減することができます。
無菌性試験およびマイコプラズマ否定試験による安全性確認
患者の体内に直接投与されるため、無菌性の保証は最優先事項です。
- 無菌試験: 細菌や真菌の混入がないことを確認します。培養法が一般的ですが、迅速法(BacT/ALERT等)の導入も進んでいます。
- マイコプラズマ否定試験: 一般的な細菌よりも検出が難しいマイコプラズマの不在を確認します。PCR法などの核酸増幅検査(NAT)が広く用いられています。
- エンドトキシン試験: 発熱物質であるエンドトキシンの量が基準値以下であることを確認します。
これらの試験は、原材料、工程途中、最終製品の各段階で適切に実施されます。
複製可能ウイルス(RCL/RCR)の検出とリスク管理
ウイルスベクターを使用する場合、ベクターが体内で複製能力を持つウイルス(RCL: Replication Competent Lentivirus / RCR: Replication Competent Retrovirus)に変化していないことを確認する必要があります。
これは製造に使用するベクター自体の品質管理に加え、最終製品や培養上清を用いた試験によって、複製可能なウイルスが存在しないことを証明します。患者の長期的な安全性を確保するために必須の項目であり、規制当局も特に注視するポイントです。
フローサイトメトリーによるCAR陽性率と純度の測定
製品中に含まれる細胞の特性を解析するために、マルチカラーフローサイトメトリーが用いられます。
- CAR陽性率: 全T細胞のうち、何%がCARを発現しているか(導入効率)。
- 細胞純度: T細胞(CD3+)の純度、およびB細胞や単球などの不純物の残存率。
- CD4/CD8比: ヘルパーT細胞とキラーT細胞の比率。
- 分化マーカー: メモリーT細胞(CD45RA, CCR7等)の割合。
これらの指標は製品の有効性と相関する可能性があり、規格値として設定されます。
細胞殺傷能力を評価するポテンシーアッセイ(効力試験)
CAR-T細胞が実際にがん細胞を攻撃する能力を持っているか、生物学的な活性を評価するのがポテンシーアッセイです。
- 細胞殺傷試験(Cytotoxicity Assay): 標的となるがん細胞と共培養し、がん細胞の死滅度合いを測定します。
- サイトカイン産生試験: 標的抗原刺激により、IFN-γやTNF-αなどのサイトカインが産生されるかを確認します。
ポテンシーアッセイは、製品のロット間の一貫性を保証するための重要な指標であり、開発段階で適切な試験系(MOA: Mechanism of Actionを反映したもの)を確立しておく必要があります。
製造コスト削減と品質安定化に向けたプロセスの最適化

CAR-T療法が広く普及するためには、製造コストの削減(CoG: Cost of Goodsの低減)と、品質の安定化が大きな課題です。これらの課題解決に向けて、現在業界で進められているプロセスの最適化アプローチについて紹介します。
オープン系から閉鎖系(クローズドシステム)への移行
従来の製造プロセスでは、安全キャビネット内での用手操作(オープン系操作)が多く含まれていました。これをチューブ溶着技術などを用いて外気と遮断された「閉鎖系(クローズドシステム)」へ移行する動きが加速しています。
閉鎖系にすることで、コンタミネーション(汚染)のリスクを劇的に低減できるだけでなく、製造区域の清浄度要件(グレード)を緩和できる可能性があります。これにより、高価なクリーンルームの維持コストや、ガウン着用などの作業負担を軽減でき、全体的な製造コスト削減に寄与します。
自動培養装置導入による人的エラーの排除と再現性向上
熟練した技術者の手技に依存するマニュアル操作は、品質のばらつきや人的エラー(ヒューマンエラー)の原因となります。これに対し、Miltenyi Biotec社のCliniMACS ProdigyやLonza社のCocoonといった「自動培養装置」の導入が進んでいます。
これらの装置は、分離、活性化、導入、培養、洗浄といった一連の工程を一つの閉鎖系デバイス内で自動実行できます。操作の標準化によりロット間の再現性が向上し、製造人員の省人化も可能になります。特に、複数の患者製品を並行して製造する際の取り違えリスク低減にも効果的です。
非ウイルスベクター技術による導入コストの低減
ウイルスベクターの製造と品質管理は、CAR-T製造コストの大きな割合(3〜4割とも言われる)を占めています。このコストを削減するため、ウイルスを使わない遺伝子導入技術の開発が進んでいます。
- トランスポゾン法(PiggyBac, Sleeping Beauty): プラスミドDNA等を用いて遺伝子を組み込む手法。
- mRNA導入: 一過性の発現にはなるが、安全性が高い手法。
- CRISPR/Cas9: ゲノム編集技術を用いた精密な遺伝子挿入。
これらの技術は、製造コストを大幅に下げるだけでなく、導入遺伝子のサイズ制限緩和や安全性の向上といったメリットも期待されており、次世代の製造プロセスとして注目されています。
製造実行システム(MES)によるデータ管理とトレーサビリティ
製造プロセスが複雑化する中で、紙ベースの記録管理は限界を迎えています。そこで、製造実行システム(MES: Manufacturing Execution System)や電子バッチ記録(EBR)の導入が進んでいます。
MESを導入することで、各工程の操作記録、機器からのデータ、原材料情報などをデジタルで一元管理できます。これにより、データの完全性(Data Integrity)が担保され、監査対応がスムーズになるだけでなく、リアルタイムでの進捗把握や在庫管理が可能になります。ミスを防止し、トレーサビリティを確実にするための基盤として、ITシステムの活用は不可欠です。
まとめ

CAR-T細胞療法の製造プロセスについて、Vein-to-Veinの全体像から各工程の技術的詳細、品質管理、そして最適化のトレンドまでを解説しました。
CAR-T製造は、単なる細胞培養ではなく、厳格なGMP管理下で行われる高度なバイオロジカルプロセスです。アフェレーシス産物の受け入れから最終製品の凍結保存に至るまで、各ステップが製品の品質(安全性・有効性)に直結しています。「Process is the Product」の原則を理解し、閉鎖系自動化デバイスやデジタル技術を活用してプロセスを最適化することは、製造コストの削減だけでなく、患者様へより高品質な治療を安定的に届けるために極めて重要です。
本記事が、貴社の製造プロセス開発や改善の一助となれば幸いです。
CAR-T製造プロセスの工程解説についてよくある質問

読者の皆様から寄せられる、CAR-T製造プロセスに関するよくある質問とその回答をまとめました。
- CAR-Tの製造期間はどのくらいかかりますか?
- 自家CAR-T療法の場合、一般的にアフェレーシス(採血)から最終製品の出荷まで2〜3週間程度かかります。これには製造工程だけでなく、無菌試験などの品質管理試験(QC)の期間も含まれます。
- 製造コストが高くなる主な要因は何ですか?
- 主な要因として、ウイルスベクターなどの高価な原材料費、高度なクリーンルーム施設の維持費、多くの人手を要する人件費、そして厳格な品質管理試験のコストが挙げられます。
- 自家CAR-Tと他家(同種)CAR-Tの製造上の違いは何ですか?
- 自家は患者ごとの「個別製造」であり、スケールアウト(並列化)が必要です。一方、他家は健康なドナーの細胞から大量に製造して保存する「大量製造」が可能で、スケールアップによるコストダウンが見込めますが、拒絶反応対策などの追加工が必要です。
- 製造プロセスでの主な失敗要因は何ですか?
- 患者由来のT細胞の状態不良(増殖しない等)、微生物汚染(コンタミネーション)、機器の故障や操作ミス、または規格外(スペックアウト)による出荷不可などが挙げられます。
- 自動化装置を導入するメリットは何ですか?
- 人的エラーの低減、閉鎖系による汚染リスクの低下、製造の再現性・安定性の向上、省人化によるコスト削減、および製造記録のデジタル化が容易になる点などが挙げられます。