がん免疫療法の領域において、「Living Drug(生きた薬)」としてパラダイムシフトをもたらしたCAR-T細胞療法。その高い奏効率は血液がん治療の新たな希望となっていますが、複雑な作用機序や拡大する適応疾患を正確に把握することは、医療従事者や製薬企業の皆様にとっても容易ではないでしょう。
本記事では、CAR-T細胞療法の詳細なメカニズムから、世代ごとの構造的進化、そして国内で承認されている最新の適応疾患までを体系的に解説します。既存の治療法との決定的な違いや、臨床現場での管理ポイントについても深く掘り下げていきますので、ぜひ日々の業務や情報収集にお役立てください。
CAR-T細胞療法とは:遺伝子改変によるがん免疫療法の到達点

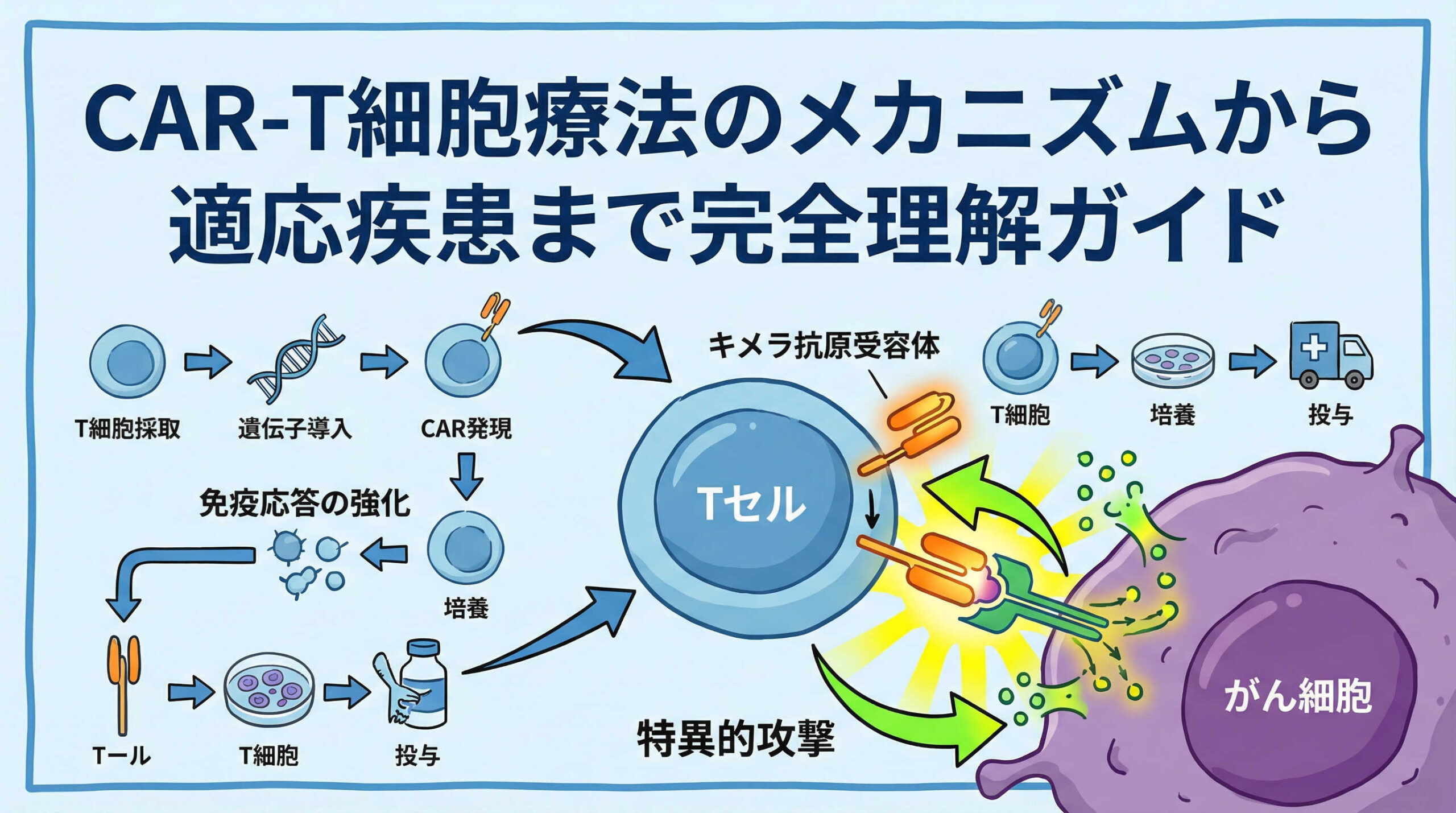
CAR-T細胞療法(Chimeric Antigen Receptor T-cell Therapy)は、患者さん自身のT細胞に遺伝子改変を施し、がん細胞を特異的に攻撃する能力を付与する画期的な治療法です。従来の化学療法や抗体医薬とは一線を画すそのメカニズムは、がん免疫療法の到達点とも言えるでしょう。ここでは、その基本的な概念と、既存治療との本質的な違いについて解説します。
既存の抗体医薬・T細胞療法との決定的な違い
CAR-T細胞療法が「生きた薬」と称される最大の理由は、投与された細胞が体内で増殖し、長期間にわたって効果を持続させる点にあります。従来の抗体医薬は血中半減期に従って濃度が低下するため、効果を維持するには反復投与が必要でした。
一方、CAR-T細胞は体内で標的抗原に出会うと活性化し、爆発的に増殖します。さらに一部はメモリーT細胞として体内に残り続けるため、がんの再発に対する長期的な監視機能も期待できるのです。このように、単なる薬剤の投与ではなく、患者さんの免疫システムそのものを強化・再構築するという点が、決定的な違いと言えるでしょう。
MHC(主要組織適合遺伝子複合体)に依存しない抗原認識メカニズム
通常、生体のT細胞が異物(がん細胞やウイルス感染細胞)を認識するためには、相手の細胞表面にあるMHC(主要組織適合遺伝子複合体)という分子に抗原ペプチドが提示されている必要があります。しかし、多くのがん細胞はこのMHCの発現を低下させ、免疫監視機構から逃れようとします。これを「免疫逃避」と呼びます。
CAR-T細胞が画期的なのは、このMHCを介さずに、がん細胞表面の抗原を直接認識できる点です。抗体由来の認識部位を持つことで、がん細胞が隠そうとしている目印をダイレクトに捉え、攻撃を仕掛けることが可能になります。これにより、従来の免疫療法では効果が得にくかった症例に対しても、強力な抗腫瘍効果を発揮することができるのです。
CAR-T細胞の構造特性と世代別メカニズムの進化

CAR-T細胞の強力な抗腫瘍効果を支えているのは、人工的に設計された「キメラ抗原受容体(CAR)」の特殊な構造です。開発初期から現在に至るまで、この構造は改良が重ねられ、より効果的で安全性の高いものへと進化してきました。ここでは、CARの基本構造と、世代ごとの機能的な違いについて詳しく見ていきましょう。
キメラ抗原受容体(CAR)の基本構造:scFvと細胞内シグナル伝達ドメイン
CAR(Chimeric Antigen Receptor)は、主に細胞外ドメイン、膜貫通ドメイン、細胞内ドメインの3つの部分から構成されています。がん細胞を認識する「眼」の役割を果たすのが細胞外ドメインにあるscFv(一本鎖抗体)であり、特定の抗原(CD19など)に結合します。
一方、攻撃のスイッチを入れるのが細胞内シグナル伝達ドメインです。ここにはT細胞受容体複合体の構成要素であるCD3ζ(ゼータ)鎖が用いられており、抗原結合のシグナルを核へと伝え、T細胞の活性化を誘導します。この「抗体の認識力」と「T細胞の殺傷力」を融合させた構造こそが、キメラ(合成)と呼ばれる所以です。
第2世代・第3世代CARにおける共刺激ドメイン(CD28/4-1BB)の役割と持続性
第1世代のCARはCD3ζ鎖のみを持っていたため、T細胞の活性化が不十分で、体内で長生きできないという課題がありました。これを克服するために開発されたのが、共刺激ドメイン(Co-stimulatory domain)を組み込んだ第2世代・第3世代のCARです。
現在承認されている製剤の多くは第2世代であり、共刺激ドメインとしてCD28または4-1BBが採用されています。
- CD28: 急速な増殖と強力な殺傷能力を誘導する傾向があります。
- 4-1BB: T細胞の疲弊を防ぎ、体内での長期生存(パーシステンス)を促すと言われています。
このドメインの違いは、各製剤の臨床的な特性や副作用の発現時期にも影響を与えるため、理解しておくことが重要です。
国内で承認されているCAR-T細胞療法の適応疾患と対象製剤

日本国内においてもCAR-T細胞療法の適応範囲は順次拡大しており、複数の製剤が薬事承認されています。現在は主に血液がん領域での使用が中心ですが、対象となる抗原や疾患のステージは製剤ごとに異なります。ここでは、現在臨床で使用可能な主な適応疾患と製剤について整理します。
CD19陽性の再発・難治性B細胞性悪性腫瘍(DLBCL・ALL等)への適応
CAR-T細胞療法が最初に成功を収め、現在も主要な適応となっているのが、B細胞性の血液がんです。B細胞の表面に特異的に発現するCD19というタンパク質を標的としています。
主な適応疾患は以下の通りです。
- 再発・難治性のびまん性大細胞型B細胞リンパ腫(DLBCL)
- 再発・難治性のB細胞性急性リンパ性白血病(B-ALL)
- 再発・難治性の濾胞性リンパ腫(FL)
これらの疾患では、標準治療が奏功しなかった場合の救済療法として、高い寛解率を示しています。特に小児や若年成人のALLにおいて、劇的な効果をもたらしたことは広く知られています。
BCMAを標的とする多発性骨髄腫に対する治療選択肢
近年、新たな標的抗原として登場したのがBCMA(B細胞成熟抗原)です。これは形質細胞に分化したB細胞に強く発現しており、多発性骨髄腫(MM)の治療ターゲットとして極めて重要です。
多発性骨髄腫は再発を繰り返す難治性の疾患ですが、プロテアソーム阻害剤、免疫調節薬、抗CD38抗体薬という主要な3クラスの薬剤に抵抗性を示した場合(Triple-class refractory)でも、BCMA標的CAR-T細胞療法は深い奏効をもたらすことが臨床試験で示されています。これにより、治療の選択肢が尽きかけた患者さんへの新たな希望となっています。
具体的な承認製剤(キムリア、イエスカルタ等)のスペック比較
現在国内で承認されている主なCAR-T製剤の特徴を比較します。それぞれ適応疾患や共刺激ドメインに違いがあります。
| 販売名 | 一般名 | 標的抗原 | 共刺激ドメイン | 主な適応 |
|---|---|---|---|---|
| キムリア | チサゲンレクルユーセル | CD19 | 4-1BB | DLBCL, B-ALL, FL |
| イエスカルタ | アキシカブタゲン シロルユーセル | CD19 | CD28 | DLBCL, FL 等 |
| ブレヤンジ | リソカブタゲン マラルユーセル | CD19 | 4-1BB | DLBCL, FL 等 |
| アベクマ | イデカブタゲン ビクルユーセル | BCMA | 4-1BB | 多発性骨髄腫 |
| カービケティ | シルタカブタゲン オートルユーセル | BCMA | 4-1BB | 多発性骨髄腫 |
製剤選択においては、患者さんの病態や、各製剤の製造期間、副作用プロファイルなどを総合的に判断する必要があります。
臨床現場における治療プロセスと製造・投与フロー

CAR-T細胞療法は、既製品の薬剤を棚から取り出して投与するものではありません。患者さん一人ひとりに合わせたオーダーメイドの治療であり、そのプロセスは高度に管理されたサプライチェーンの上で成り立っています。ここでは、患者さんから細胞を採取し、製品として戻ってくるまでの流れと、投与前の重要な処置について解説します。
アフェレーシス(成分採血)による患者T細胞の採取
治療の第一歩は、原料となるT細胞の確保です。これをアフェレーシス(成分採血)と呼びます。専用の機器を用いて患者さんの血液を体外循環させ、必要な白血球(リンパ球)分画のみを採取し、残りの成分(赤血球や血漿など)は体内に戻します。
この工程では、十分な数の健全なT細胞を採取することが重要です。そのため、直前の化学療法による骨髄抑制からの回復状況や、血中のリンパ球数などを事前に厳密に確認します。採取された細胞は、厳格な温度管理下で製造施設へと空輸されます。
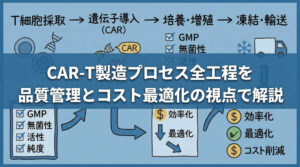
ウイルスベクターを用いた遺伝子導入とex vivoでの培養・増幅
製造施設に到着したT細胞は、活性化された後、ウイルスベクター(レンチウイルスやレトロウイルスなど)を用いてCAR遺伝子を導入されます。これにより、T細胞はCAR-T細胞へと生まれ変わります。
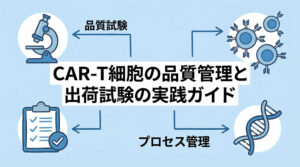
その後、臨床で使用できる数(数億個レベル)になるまでex vivo(体外)で培養・増幅されます。このプロセスには通常数週間を要します。最後に厳格な品質試験(無菌試験、力価試験など)をクリアしたものだけが、最終製品として凍結保存され、医療機関へと返送されます。この「待ち時間」の間、患者さんの病勢をコントロールするブリッジング治療が重要となることもあります。
投与前のリンパ球除去化学療法とその免疫学的意義
製品が届き、いよいよ投与となる数日前に実施されるのがリンパ球除去化学療法です。一般的にはフルダラビンとシクロホスファミドの併用療法が行われます。
この処置には、単に腫瘍を減らすだけでなく、免疫学的に重要な意義があります。
- 患者体内の制御性T細胞(Treg)などの抑制性細胞を減らし、CAR-T細胞が働きやすい環境を作る。
- 恒常性維持サイトカイン(IL-7やIL-15など)の血中濃度を高め、投与されたCAR-T細胞の増殖を助ける。
つまり、CAR-T細胞という「種」を撒く前に、体という「畑」を耕すための必須の工程と言えるでしょう。
投与管理において注意すべき特有の副作用(AE)

高い治療効果の一方で、CAR-T細胞療法には特有の重篤な副作用が存在します。これらは免疫系の過剰な活性化に起因するものであり、従来の抗がん剤の副作用とは対処法が異なります。医療チームによる早期発見と適切な介入が、患者さんの予後を左右すると言っても過言ではありません。
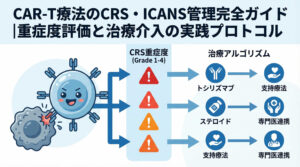
サイトカイン放出症候群(CRS)の病態生理とトシリズマブ投与基準
サイトカイン放出症候群(CRS)は、CAR-T細胞が活性化・増殖する過程で大量の炎症性サイトカインが放出されることで起こる全身性の炎症反応です。発熱から始まり、重症化すると低血圧、低酸素症、多臓器不全に至る可能性があります。
CRSの病態において中心的な役割を果たすのがインターロイキン-6(IL-6)です。そのため、CRSの管理には抗IL-6受容体抗体であるトシリズマブが特効薬として用いられます。各施設のアルゴリズムに基づき、グレードに応じた適切なタイミングでの投与が推奨されています。
免疫エフェクター細胞関連神経毒性症候群(ICANS)の発現機序とモニタリング
もう一つの特徴的な副作用が、免疫エフェクター細胞関連神経毒性症候群(ICANS)です。頭痛や振戦、言語障害(失語)、意識障害などを呈します。重症例では脳浮腫に至ることもあり、厳重なモニタリングが必要です。
ICANSの早期発見には、毎日同じ文章を書かせる「筆記テスト」や、ICEスコアなどの評価ツールが有用です。ICANSに対してはトシリズマブの効果が限定的であるため、血液脳関門を通過できるステロイド剤の投与が治療の中心となります。CRSとは異なる病態メカニズムであることを理解し、神経症状の変化を見逃さないことが肝要です。
現在の課題と次世代CAR-T細胞開発の展望

CAR-T細胞療法は血液がんにおいて革新的な成果を上げましたが、まだ解決すべき課題も残されています。特に固形がんへの応用や、製造コスト・期間の問題は、世界中で活発に研究が進められているテーマです。最後に、次世代のCAR-T細胞開発に向けた展望について触れます。
固形がんへの適応拡大を阻む腫瘍微小環境(TME)の壁
血液がんと異なり、固形がん(胃がんや肺がんなど)に対するCAR-T細胞療法の効果は限定的です。最大の障壁は腫瘍微小環境(TME)です。TMEは物理的な壁としてCAR-T細胞の浸潤を阻むだけでなく、免疫抑制性のシグナルを出してT細胞の機能を低下させます。
この壁を突破するため、PD-1などの免疫チェックポイント分子を阻害する機能を付加した「Armored CAR(武装CAR)」や、固形がん特有の抗原を標的とする新たなCARの開発が進められています。TMEを攻略できるかどうかが、適応拡大の鍵となるでしょう。
製造コスト削減と即時投与を目指す他家(Off-the-shelf)CAR-Tの開発
現在のCAR-Tは患者自身の細胞を使う「自家移植」であるため、製造に時間とコストがかかります。これを解決するために期待されているのが、健康なドナーの細胞やiPS細胞からあらかじめ大量に製造しておく他家(Off-the-shelf)CAR-Tです。
他家細胞を用いる場合、患者さんへの拒絶反応(GvHD)が懸念されますが、CRISPR/Cas9などのゲノム編集技術を用いてTCR(T細胞受容体)を除去することで、そのリスクを回避する研究が進んでいます。実用化されれば、「必要な時にすぐに投与できる」治療となり、コストも大幅に削減できる可能性があります。
まとめ

本記事では、CAR-T細胞療法のメカニズムから適応疾患、そして臨床上の課題までを包括的に解説しました。
CAR-T細胞療法は、従来の「薬」の概念を超え、患者自身の免疫細胞を遺伝子工学的に強化してがんと戦わせる革新的な治療法です。MHCに依存しない直接的な抗原認識と、体内での増殖・持続性は、難治性の血液がんにおいて高い奏効率を実現しました。
一方で、CRSやICANSといった特有の副作用管理、複雑な製造プロセス、そして固形がんへの適応拡大など、向き合うべき課題も明確です。日進月歩で進化するこの領域において、最新の知見をアップデートし続けることが、私たち医療・製薬業界に携わる者の責務と言えるでしょう。
CAR-T細胞療法のメカニズムと適応疾患についてよくある質問

FAQセクション